结直肠癌(Colorectal cancer,CRC)发病率和死亡率较高,威胁人类生命健康。作为治疗转移性CRC的一线药物,化疗药物卡培他滨(Capecitabine,Cap)具有肿瘤特异性毒性和高响应率等优势,但其血浆半衰期极短,需要每天两次高剂量给药,导致剂量相关毒性。因此,开发能够有效延缓其血浆清除的递送系统对提高Cap的临床疗效至关重要。
CRC的发生发展与肠道微生物群密切相关,部分益生菌被报道具有增强宿主抗肿瘤免疫应答的作用,部分有害菌则与CRC进展和治疗耐药相关。以木聚糖为代表的益生元可以被益生菌消化代谢,提高肠道有益菌的比例,且自身具有良好的生物相容性,使其具备成为化疗药物递送载体材料的潜力。
中国科学院上海药物研究所李亚平课题组在《自然-通讯》(Nature Communications)上,发表了题为Combining gut microbiota modulation and chemotherapy by capecitabine-loaded prebiotic nanoparticle improves colorectal cancer therapy的研究论文。
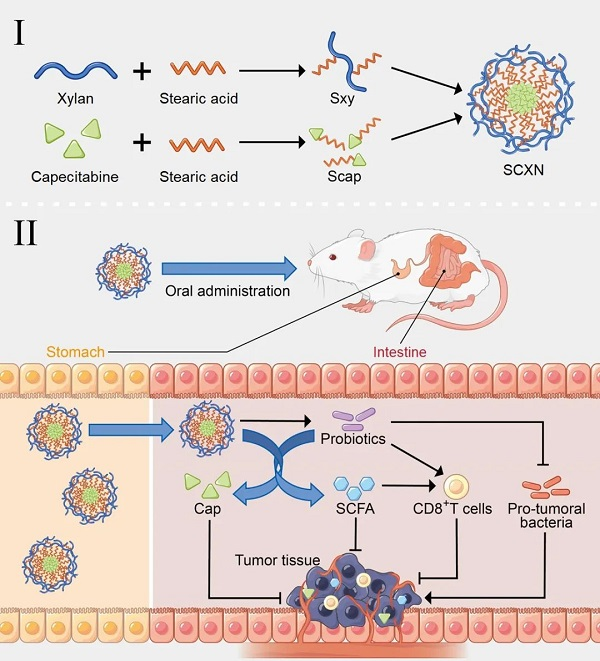
该研究合成了两亲性的木聚糖-硬脂酸偶联物(Sxy)。Sxy在水中可自组装形成纳米粒,并将硬脂酸修饰的Cap包裹在纳米粒内核中,获得载Cap益生元纳米粒SCXN。研究显示,口服给药后,SCXN在胃部稳定,在肠道特定细菌的作用下,木聚糖逐渐降解,纳米粒解离并持续释放Cap,与游离药相比可减缓Cap被小肠吸收进入血液循环的速度,减慢清除,增加瘤内蓄积,提高肿瘤细胞杀伤效率。同时,木聚糖降解后提高了肠道益生菌比例,降低了致癌菌比例,增加了有益代谢物短链脂肪酸的含量。研究在荷CT26及MC38结肠癌小鼠模型中开展的药效评价结果表明,与游离Cap相比,SCXN口服后增加了瘤内CD8+T细胞数量,减少了调节性T细胞数量,增强了抗肿瘤免疫应答,肿瘤抑制率从5.29%提高至71.78%。此外,SCXN具有良好的生物相容性,可使结肠癌模型小鼠的中位生存期从14天延长至33.5天。该基于益生元的肠道菌群调节-化疗一体化纳米递送系统有望为CRC治疗提供新策略。
研究工作得到国家重点研发计划、国家自然科学基金、山东省自然科学基金和上海市“扬帆计划”等的资助。张江实验室国家蛋白质科学研究(上海)设施和上海药物所冷冻电镜研究中心在实验中对本研究予以支持。